摘要:研究人員發(fā)現(xiàn),驅(qū)動癌癥的蛋白MYC也會抑制免疫警報信號,使腫瘤在不被注意的情況下生長。當這種免疫屏蔽能力在動物模型中失效時,腫瘤迅速瓦解。
這一發(fā)現(xiàn)會改變未來癌癥的治療方式嗎?在實驗室研究中,答案似乎很有希望。一個國際科學家團隊發(fā)現(xiàn)了一個關鍵的生物學過程,幫助胰腺癌生長并逃避免疫系統(tǒng)。通過破壞這一過程,研究人員能夠在動物實驗中顯著縮小腫瘤。
這些發(fā)現(xiàn)揭示了癌細胞保護自己免受免疫攻擊的主要方式。當這種保護機制被阻斷時,實驗動物體內(nèi)的腫瘤迅速瓦解,這表明在一種最致命的癌癥中存在一種強大的新弱點。
已發(fā)表的研究結(jié)果和全球合作
這項研究發(fā)表在《細胞》雜志上,由一個國際研究小組領導。大部分實驗工作是由 Leonie Uhl、Amel Aziba和Sinah L?bbert以及來自烏爾茨堡大學(JMU)、麻省理工學院(美國)和烏爾茨堡大學醫(yī)院的合作者共同完成的。

圖1 MYC與新生RNA結(jié)合通過抑制R-loop衍生的RNA-DNA雜交體來抑制先天免疫信號傳導
JMU生物化學和分子生物學主席Martin Eilers作為癌癥大挑戰(zhàn)KOODAC*團隊的一部分領導了這項研究。資金支持來自英國癌癥研究中心、兒童無癌基金會(Kika)和法國國家癌癥研究所(INCa)通過癌癥大挑戰(zhàn)倡議。額外的資金由歐洲研究委員會授予Eilers的高級補助金提供。
驅(qū)動癌癥生長的蛋白質(zhì)
研究人員專注于MYC,一種在癌癥生物學中已經(jīng)研究了幾十年的蛋白質(zhì)。MYC被稱為癌蛋白,因為它在推動細胞分裂方面起著重要作用?!霸谠S多類型的腫瘤中,這種蛋白質(zhì)是細胞分裂的核心驅(qū)動因素之一,因此是不受控制的腫瘤生長,”Eilers解釋說。
目前尚不清楚具有非常高MYC活性的腫瘤是如何避免被免疫系統(tǒng)檢測到的。盡管生長迅速,但myc驅(qū)動的腫瘤往往無法引發(fā)免疫反應,從而使其不受控制地擴散。
MYC在壓力下扮演第二角色
這項新研究提供了一個答案。研究人員發(fā)現(xiàn)MYC有兩種不同的功能。在正常情況下,MYC與DNA結(jié)合并開啟促進細胞生長的基因。但是在快速生長的腫瘤內(nèi)部的壓力環(huán)境中,MYC改變了它的行為。
MYC不再附著在DNA上,而是開始與新產(chǎn)生的RNA分子結(jié)合。這種轉(zhuǎn)變導致多個MYC蛋白聚集在一起,形成稱為多聚體的密集組,其作用類似于分子凝聚體。
這些凝聚體在細胞內(nèi)起聚集作用,吸收其他蛋白質(zhì),尤其是外泌體復合物,并將它們集中在一個地方。
使細胞內(nèi)部警報系統(tǒng)靜音
外泌體復合體在細胞內(nèi)起著清理作用。在這種情況下,它選擇性地分解RNA-DNA雜交體,這是基因活動的錯誤副產(chǎn)品。正常情況下,這些雜交體充當了求救信號,提醒免疫系統(tǒng)細胞內(nèi)部出了問題。
通過組織摧毀這些雜交體,MYC在激活免疫防御之前有效地關閉了警報系統(tǒng)。因此,信號傳遞過程從未開始,免疫細胞無法將腫瘤視為威脅。
一個單獨的功能,使免疫逃避
研究小組表明,這種免疫隱藏能力依賴于MYC蛋白中特定的RNA結(jié)合區(qū)域。重要的是,這個區(qū)域不需要MYC在驅(qū)動細胞生長中的作用,這意味著這兩種功能獨立運作。
研究人員證明,MYC促進腫瘤生長的能力和抑制免疫檢測的能力在機制上是不同的過程。
當盾牌被移除時,腫瘤會崩潰
為了測試其影響,科學家們改變了MYC,使其不再與RNA結(jié)合。如果沒有這種功能,MYC就不能招募外泌體復合物或抑制免疫警報。
動物模型的結(jié)果是驚人的。“具有正常MYC的胰腺腫瘤在28天內(nèi)增大了24倍,而具有缺陷MYC蛋白的腫瘤在同一時期內(nèi)崩潰并縮小了94%,但前提是動物的免疫系統(tǒng)完好無損,”Eilers說。
這證實了免疫活動對腫瘤的崩潰至關重要。
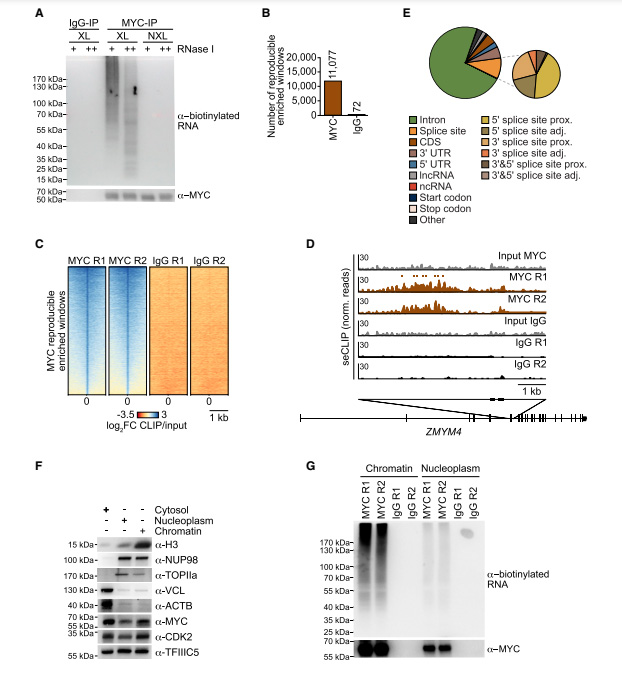
圖2 MYC結(jié)合新生RNA
未來治療的更精確目標
這一發(fā)現(xiàn)為癌癥治療開辟了新的可能性。過去試圖完全關閉MYC的努力都失敗了,因為這種蛋白質(zhì)對健康細胞也至關重要。將其廣泛靶向可能會導致嚴重的副作用。
新確定的機制提供了一種更有針對性的方法。未來的藥物可以特異性地抑制MYC結(jié)合RNA的能力,而不是完全關閉MYC。Eilers解釋說:“這可能會使其促進生長的功能保持不變,但會解除腫瘤的隱形斗篷?!边@可以讓免疫系統(tǒng)識別并再次攻擊癌癥。
接下來會發(fā)生什么?
盡管前景光明,但研究人員警告說,臨床應用還很遙遠。未來的工作將需要確定免疫激活RNA-DNA雜交體如何離開細胞核,以及MYC的RNA結(jié)合活性如何塑造腫瘤的局部環(huán)境。
癌癥重大挑戰(zhàn)項目主任David Scott博士強調(diào)了這項工作的廣泛意義:“癌癥重大挑戰(zhàn)項目的存在是為了支持像KOODAC這樣的國際團隊,他們正在推動我們對癌癥的了解。這樣的研究表明,揭示腫瘤用來躲避免疫系統(tǒng)的機制可以為成人癌癥和兒童癌癥開辟新的可能性,這是KOODAC團隊關注的重點。這是一個令人鼓舞的例子,說明國際合作和多樣化的專業(yè)知識如何有助于解決癌癥研究中一些最棘手的挑戰(zhàn)。
關于癌癥大挑戰(zhàn)
癌癥大挑戰(zhàn)由英國癌癥研究所和國家癌癥研究所于2020年成立,匯集了來自世界各地的領先研究團隊,以解決癌癥科學中最困難的問題。這些挑戰(zhàn)過于復雜,任何一個機構(gòu)或國家都無法單獨解決。
該項目提供高達2000萬英鎊的資助,使團隊能夠跨越傳統(tǒng)的科學和地理界限,加速抗癌的進展。
參考資料
[1] Amyloid-β and Tau in Alzheimer’s disease: pathogenesis, mechanisms, and interplay
摘要:研究人員發(fā)現(xiàn),驅(qū)動癌癥的蛋白MYC也會抑制免疫警報信號,使腫瘤在不被注意的情況下生長。當這種免疫屏蔽能力在動物模型中失效時,腫瘤迅速瓦解。
這一發(fā)現(xiàn)會改變未來癌癥的治療方式嗎?在實驗室研究中,答案似乎很有希望。一個國際科學家團隊發(fā)現(xiàn)了一個關鍵的生物學過程,幫助胰腺癌生長并逃避免疫系統(tǒng)。通過破壞這一過程,研究人員能夠在動物實驗中顯著縮小腫瘤。
這些發(fā)現(xiàn)揭示了癌細胞保護自己免受免疫攻擊的主要方式。當這種保護機制被阻斷時,實驗動物體內(nèi)的腫瘤迅速瓦解,這表明在一種最致命的癌癥中存在一種強大的新弱點。
已發(fā)表的研究結(jié)果和全球合作
這項研究發(fā)表在《細胞》雜志上,由一個國際研究小組領導。大部分實驗工作是由 Leonie Uhl、Amel Aziba和Sinah L?bbert以及來自烏爾茨堡大學(JMU)、麻省理工學院(美國)和烏爾茨堡大學醫(yī)院的合作者共同完成的。

圖1 MYC與新生RNA結(jié)合通過抑制R-loop衍生的RNA-DNA雜交體來抑制先天免疫信號傳導
JMU生物化學和分子生物學主席Martin Eilers作為癌癥大挑戰(zhàn)KOODAC*團隊的一部分領導了這項研究。資金支持來自英國癌癥研究中心、兒童無癌基金會(Kika)和法國國家癌癥研究所(INCa)通過癌癥大挑戰(zhàn)倡議。額外的資金由歐洲研究委員會授予Eilers的高級補助金提供。
驅(qū)動癌癥生長的蛋白質(zhì)
研究人員專注于MYC,一種在癌癥生物學中已經(jīng)研究了幾十年的蛋白質(zhì)。MYC被稱為癌蛋白,因為它在推動細胞分裂方面起著重要作用?!霸谠S多類型的腫瘤中,這種蛋白質(zhì)是細胞分裂的核心驅(qū)動因素之一,因此是不受控制的腫瘤生長,”Eilers解釋說。
目前尚不清楚具有非常高MYC活性的腫瘤是如何避免被免疫系統(tǒng)檢測到的。盡管生長迅速,但myc驅(qū)動的腫瘤往往無法引發(fā)免疫反應,從而使其不受控制地擴散。
MYC在壓力下扮演第二角色
這項新研究提供了一個答案。研究人員發(fā)現(xiàn)MYC有兩種不同的功能。在正常情況下,MYC與DNA結(jié)合并開啟促進細胞生長的基因。但是在快速生長的腫瘤內(nèi)部的壓力環(huán)境中,MYC改變了它的行為。
MYC不再附著在DNA上,而是開始與新產(chǎn)生的RNA分子結(jié)合。這種轉(zhuǎn)變導致多個MYC蛋白聚集在一起,形成稱為多聚體的密集組,其作用類似于分子凝聚體。
這些凝聚體在細胞內(nèi)起聚集作用,吸收其他蛋白質(zhì),尤其是外泌體復合物,并將它們集中在一個地方。
使細胞內(nèi)部警報系統(tǒng)靜音
外泌體復合體在細胞內(nèi)起著清理作用。在這種情況下,它選擇性地分解RNA-DNA雜交體,這是基因活動的錯誤副產(chǎn)品。正常情況下,這些雜交體充當了求救信號,提醒免疫系統(tǒng)細胞內(nèi)部出了問題。
通過組織摧毀這些雜交體,MYC在激活免疫防御之前有效地關閉了警報系統(tǒng)。因此,信號傳遞過程從未開始,免疫細胞無法將腫瘤視為威脅。
一個單獨的功能,使免疫逃避
研究小組表明,這種免疫隱藏能力依賴于MYC蛋白中特定的RNA結(jié)合區(qū)域。重要的是,這個區(qū)域不需要MYC在驅(qū)動細胞生長中的作用,這意味著這兩種功能獨立運作。
研究人員證明,MYC促進腫瘤生長的能力和抑制免疫檢測的能力在機制上是不同的過程。
當盾牌被移除時,腫瘤會崩潰
為了測試其影響,科學家們改變了MYC,使其不再與RNA結(jié)合。如果沒有這種功能,MYC就不能招募外泌體復合物或抑制免疫警報。
動物模型的結(jié)果是驚人的?!熬哂姓YC的胰腺腫瘤在28天內(nèi)增大了24倍,而具有缺陷MYC蛋白的腫瘤在同一時期內(nèi)崩潰并縮小了94%,但前提是動物的免疫系統(tǒng)完好無損,”Eilers說。
這證實了免疫活動對腫瘤的崩潰至關重要。

圖2 MYC結(jié)合新生RNA
未來治療的更精確目標
這一發(fā)現(xiàn)為癌癥治療開辟了新的可能性。過去試圖完全關閉MYC的努力都失敗了,因為這種蛋白質(zhì)對健康細胞也至關重要。將其廣泛靶向可能會導致嚴重的副作用。
新確定的機制提供了一種更有針對性的方法。未來的藥物可以特異性地抑制MYC結(jié)合RNA的能力,而不是完全關閉MYC。Eilers解釋說:“這可能會使其促進生長的功能保持不變,但會解除腫瘤的隱形斗篷。”這可以讓免疫系統(tǒng)識別并再次攻擊癌癥。
接下來會發(fā)生什么?
盡管前景光明,但研究人員警告說,臨床應用還很遙遠。未來的工作將需要確定免疫激活RNA-DNA雜交體如何離開細胞核,以及MYC的RNA結(jié)合活性如何塑造腫瘤的局部環(huán)境。
癌癥重大挑戰(zhàn)項目主任David Scott博士強調(diào)了這項工作的廣泛意義:“癌癥重大挑戰(zhàn)項目的存在是為了支持像KOODAC這樣的國際團隊,他們正在推動我們對癌癥的了解。這樣的研究表明,揭示腫瘤用來躲避免疫系統(tǒng)的機制可以為成人癌癥和兒童癌癥開辟新的可能性,這是KOODAC團隊關注的重點。這是一個令人鼓舞的例子,說明國際合作和多樣化的專業(yè)知識如何有助于解決癌癥研究中一些最棘手的挑戰(zhàn)。
關于癌癥大挑戰(zhàn)
癌癥大挑戰(zhàn)由英國癌癥研究所和國家癌癥研究所于2020年成立,匯集了來自世界各地的領先研究團隊,以解決癌癥科學中最困難的問題。這些挑戰(zhàn)過于復雜,任何一個機構(gòu)或國家都無法單獨解決。
該項目提供高達2000萬英鎊的資助,使團隊能夠跨越傳統(tǒng)的科學和地理界限,加速抗癌的進展。
參考資料
[1] Amyloid-β and Tau in Alzheimer’s disease: pathogenesis, mechanisms, and interplay



